目次
実験目的
導入
動物の取り扱い
RI 標識化合物
投与液の調製
投与ルート
試料中放射能の測定
ADME 試験内容
最後に
実験目的
ラット、マウス等の小動物で、H-3、C-14 を用いてADME(Absorption(吸収)、Distribution(分布)、Metabolism(代謝)、Excretion(排泄))を調べる。
導入
薬物の体内での動態試験(ADME)はその薬理及び毒性の発現を考える上で重要な試験である。RI を使用せずにADME を調べるには、薬物特異的な化学特性を明らかにして、薬物と生体内物質(内因性物質)を分離分析する技術が必要となり、代謝物も含めた薬物の動きを定量的にトレース(追跡)するのは困難な場合が多い。薬物に特異性を与えるという観点から、RI 標識は非常に優れた方法であり、RI 標識した化合物を動物に投与してその動態を調べる方法が一般的かつ標準的となっている。
基本的な動態試験は、RI 標識化合物を動物に投与して、経時的に血液、組織、尿及び糞(必要に応じて呼気)の放射能を測定し放射能の中身(未変化体もしくは代謝物)を評価する操作となる。投与する化合物の比放射能と生体から採取した試料の重量(容量)とその放射能から、生体試料中の代謝物を含む化合物濃度と量、投与量に対する割合を計算して動物における化合物の体内動態を定量的に評価することができる。
動物の取り扱い
近年は動物実験の3R(Replacement:代替法の利用、Reduction:使用動物数の削減、Refinement:苦痛軽減を中心とする動物実験・環境の洗練)が原則となっており、動物福祉や倫理を考慮した人道的観点から十分注意して動物実験を行う必要がある。ADME 試験を行う者は、特に動物実験手技に習熟し、動物に苦痛等を与えないよう配慮する必要がある。
RI 標識化合物
新規化合物の動態を調べる場合、化合物構造内で代謝的に安定な位置(代謝されない位置)に標識するよう合成経路等を検討する。標識化合物の比放射能は、RI の自己分解も考慮し適切な値となるよう配慮する。
また、当然の事ながら放射化学的純度が悪いと、RI標識された分解物等も含めて動物に投与することになり、生体試料中の放射能が未変化体由来の代謝物なのか分解物等由来の代謝物なのかを見極める過程が生じる為、95%より高い放射化学的純度の標識化合物を使用するようにする。
投与液の調製
目的とする投与放射能量及び投与化合物量になるように、RI 標識化合物と非標識化合物を混合して投与液を調製する。投与液の比放射能(放射能量/化合物量)は、試験内容、投与ルート、採取測定する試料量、必要な検出下限、測定機器の検出感度を考慮して決定する。
通常、生体試料中放射能を液体シンチレーションカウンター(以下の測定の項で説明)により測定する場合、動物体重当たりで2~10 MBq/kg 程度の放射能を目安とするが、イメージングプレート(以下の測定の項で説明)による測定の場合、H-3 体は約10 倍の放射投与量を目安とする。どのような場合においても、下限数量(H-3:1,000 MBq、C-14:10 MBq)を超えないような投与、実験を計画する必要がある。
投与ルート
種々の投与ルートがあり、実験の目的に応じたルートを採用する。
経口投与
小動物用胃ゾンデを用い直接動物の胃内へ化合物溶液を投与する。
静脈内投与
ラット、マウスの尾静脈もしくは大腿静脈等に化合物溶液(生理食塩水溶液)を注射する。
その他
皮下投与、筋肉内投与、気管内投与、経皮投与、点眼投与、十二指腸内投与、直腸内投与 等
試料中放射能の測定
H-3、C-14 の場合、液体シンチレーションカウンター(LSC)での測定が基本となる。本測定は試料がバイアル中で溶解していることが必要で、試料溶解液に液体シンチレーターを加えて測定する。このため、試料が固体等の場合は下記に示すようなどちらかの前処理を行い、また、最終測定試料が着色しているとクエンチングにより測定が困難になるため必要に応じて脱色処置等も行う。市販の液体シンチレーションカクテル剤はその試料に応じた適切なものを使用する。

液体シンチレーションカウンタ
溶解法
バイアル内に試料を分取し、組織溶解剤を加えて加温溶解させ、血液等の場合はH2O2 で脱色してからシンチレーターを加えてLSC で測定する。
燃焼法
サンプルオキシダイザー(試料燃焼によりH-3 を3H2O、C-14 を14CO2 として気化後に溶媒中に溶解して回収する装置)によりRI を液化してLSC で測定する。
ADME 試験内容
吸収試験
新規化合物が消化管から吸収され門脈まで到達するかを定量的に評価する試験で、RI標識化合物を、胆管カニュレーションを施した動物に経口投与後、胆汁、尿及び糞を分離して回収し、投与量に対する胆汁と尿中に排泄された放射能量の比(吸収率 Fa)を算出する。また、無処理動物にRI 標識化合物を経口投与し、尿と糞を分離して回収し、投与量に対する尿中の放射能量の比(尿中排泄率)も算出しておく。Fa と尿中回収率に差が生じる場合、腸肝循環(胆汁中に排泄された未変化体もしくは抱合された代謝物が腸内細菌で脱抱合され、再び消化管から吸収されること)の可能性がある。
新規化合物の非標識体もしくはRI 標識体を用いて、動物に経口及び静脈内投与後の血漿中未変化体を液体クロマトグラフ-タンデム質量分析計(LC/MS/MS)で定量し、その濃度推移から、無限大時間までの血漿中濃度-時間曲線下面積(AUCinf)を算出し、経口投与時のそれを静脈内投与時のそれで徐した値は、生物学的利用率(F)と呼ばれる。経口投与された新規化合物が消化管から吸収され門脈血から肝臓に到達したにも関わらず、代謝されたり胆汁中に排泄されたりし、抹消血にまで到達しない場合、F<Fa となる。

一般的な血中濃度曲線
分布試験
組織摘出により組織内濃度を測定する方法と、全身オートラジオグラフィーにより放射能の全身分布画像を撮り組織内濃度を測定する方法がある。RI 標識体として定量する為、代謝物を含む分布を観察していることに注意する。
①組織摘出法
RI 標識化合物投与後の動物について、所定の時間に麻酔下における全採血により安楽死させる。所定の各組織の全部あるいは一部を採取し、その重量を測定して、先の方法で組織を溶解し、シンチレーターを加えて組織内放射能をLSC で測定する。
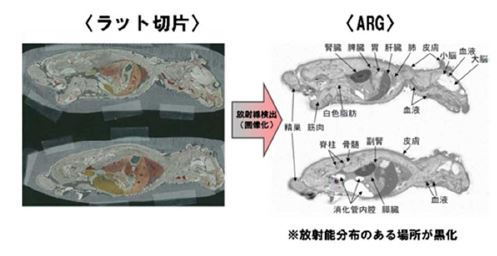
②全身オートラジオグラフィー
RI 標識化合物投与後の動物について、所定の時間に安楽死させる。全身を剃毛し、CMC(カルボキシメチルセルロース)ペーストに包埋して速やかにドライアイス-ヘキサン(あるいはアセトン)等に浸漬して凍結させる。
大型滑走式凍結ミクロトームを用いて、30 μm 厚程度の凍結切片を作成し、切片を冷凍庫内で凍結乾燥させる。乾燥後の切片は専用のルミナー膜で覆い(C-14)、イメージングアナライザー用のイメージングプレート(IP)に所定の方法で必要な時間密着する。なお、H-3 については、エネルギーが低いため切片を直接H-3 用のIP に密着する。また、得られる画像により組織内濃度を測定する場合には、RI 検量線を得るため標準試料も切片と共に密着させる。
IP をイメージングアナライザーで読み取り、全身オートラジオグラフィー(ARG)を得て、必要に応じてその画像標準検量線から組織内濃度を測定する。

大型滑走式凍結ミクロトーム

イメージングアナライザー
代謝試験
RI 標識化合物投与後の動物から、血漿、尿、糞、胆汁、組織等を採取し、その中のRI標識化合物由来の代謝物を検索し、代謝物の構造をLC-MS/MS 等で推定もしくは同定し、必要に応じてそれらを定量する。更に、代謝物の生成をin vitro 条件下(肝細胞や組織細胞画分を用いて)で実施し、関与する代謝酵素の分布するオルガネラを評価し、代謝酵素を推定する。
代謝物の構造を推定し同定する為に、以前は、複数の動物にRI 標識体を複数回投与して代謝物を多く含む生体試料を集め、薄層クロマトグラフィーや逆相オープンカラム等で当該代謝物を精製した。今日では、生体試料からの分離技術(液体クロマトグラフィー)と構造情報を得る為の質量分析(MS)装置の性能が飛躍的に向上した為、代謝物を精製することは無くなったものの、RI 標識化合物を用いることで代謝物を追うという操作は変わらない。
排泄試験
RI 標識化合物投与後の動物を代謝ケージ内で飼育し、自然排泄された尿、糞及び呼気を経時的に分離回収する。回収した尿及び呼気回収液はその容量を測定し、一定量をLSCで測定する。糞はホモジナイズ等で均一化した後に、一定量を溶解してLSC で測定する。
原則、排泄率曲線がプラトーになり、投与放射能がほぼ排泄されるまで試料を採取測定する。
胆汁中排泄試験を行う場合、予め胆管にポリエチレンチューブのカニューレ措置を行ったラットにRI 標識化合物を投与後、経時的に胆汁を回収し、胆汁中放射能をLSC で測定する。マウスには胆嚢があり胆管が細くカニューレ措置が困難であるためその手法は関係論文等を参照する。
排泄試験は排泄物を回収する試験であるものの、意味するところは、吸収性評価(A)、親化合物の体内消失に占める代謝の寄与の評価(M)等、ADME 試験において重要な位置を占める。

代謝ケージ

排泄率曲線
最後に
本項では、マウス、ラットにおけるRI 標識化合物を用いる一般的なADME 試験の概要についてのみ記載したが、薬物の体内動態試験(ADME)は、医薬品開発における臨床評価においても重要な試験(human hot study、ヒトマスバランス試験、ヒトAME 試験)であり、実施する内容はほぼ同じである。
動物用に合成したRI 標識体の合成経路を基にヒト試験用のRI 標識体を合成し、安定性及び比放射能を確認後に、ヒトに投与する。一定期間、尿と糞を回収し、採血する。動物で得た代謝物の知見を基に、ヒト血漿、尿、及び糞試料を用いてヒトの代謝物プロファイルを定量的に評価する。
また、新規化合物が承認申請にまで到達した場合には、非臨床ADME として上記試験に加え、RI 標識化合物を用いてin vitro で実施するヒトを含む各種の血漿蛋白結合率や血球移行性、ラット等を用いたin vivo で評価する乳汁移行性及び胎盤通過性試験は必須となる。詳細な手技は関係論文や書籍等を参照すること。
